最畅销艾滋病药Truvada首个仿制药获FDA批准上市
FDA6月8日批准了Teva公司生产的恩曲他滨/富马酸替诺福韦二吡呋酯片200,300mg上市,用于联合其他抗逆转录病毒药物治疗成人及儿童HIV-1感染以及成人高危人群的HIV暴露前预防。Teva未对仿制版Truvada获批上市的消息发表评论,也未透露其具体价格。
Truvada最早在2004年8月被FDA批准上市,联合其他抗逆转录病毒药物治疗HIV-1感染,2012年被FDA批准用于预防性传播导致的成人获得性HIV-1感染。不过由于遭受了Truvada可导致不安全性行为增多的指责,Gilead刚开始并未大力推广Truvada用于暴露前预防,一直到2014年美国CDC对Truvada的这个用法做出正式推荐,Gilead才开始大力推广此适应症。据Gilead透露,2017年第1季度大约有12.5万人在使用Truvada。
Truvada不是Gilead各种hiv药中最销量排行的的,也是现在截止欧洲最销量排行的hiv药。2020年英国市扬售卖薪资收入来源24亿元,欧洲售卖薪资收入来源3五亿元。
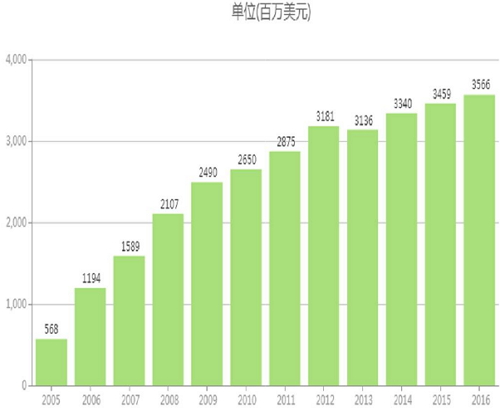
吉利汽车德Truvada世界各国销量额(百来万人民币)
没过Truvada的2017Q1的澳大利亚行业市场业务员效益为4.64亿澳元,相较于2016Q1的5.75亿澳元有较显著下挫,重点是因此TAF做重点成分表的艾滋病毒抗癌新药悄然纳斯达克上市已经的竞争队友GSK的显著涉足。
Teva的恩曲他滨/富马酸替诺福韦二吡呋酯片上市后,会凭借价格优势覆盖更多的人群,但目前尚无法预测Truvada仿制药的准确上市时间,Gilead已经对Lupin、Cipla、Amneal制药公司的Truvada仿制申请提起了专利侵权诉讼。

分享到:







 一些内容
一些内容